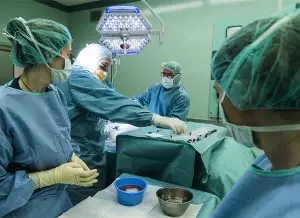
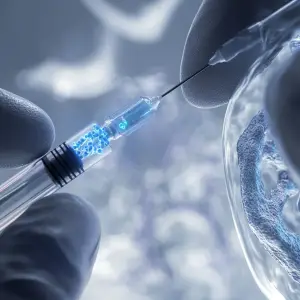
En el ámbito de las intervenciones biológicas musculoesqueléticas, es frecuente encontrar procedimientos que utilizan aspirados medulares concentrados aplicados el mismo día junto a desarrollos basados en células mesenquimales cultivadas (CMC). Aunque ambos enfoques comparten un origen biológico común —la médula ósea o el tejido adiposo—, su naturaleza científica y regulatoria es sustancialmente distinta.
Los concentrados celulares del mismo día corresponden a productos mínimamente manipulados, mientras que las células mesenquimales cultivadas constituyen el principio activo de un medicamento de terapia celular avanzada, fabricado en sala blanca bajo normativa GMP, con dosis definida, caracterización celular y control por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). La diferencia no radica únicamente en el tejido de origen, sino en el proceso de expansión ex vivo y en su estatus jurídico como medicamento.
Comprender esta distinción no es una cuestión terminológica, sino científica y normativa. Implica diferenciar entre un procedimiento biológico y un medicamento desarrollado bajo estándares farmacéuticos europeos, con implicaciones directas en trazabilidad, evidencia clínica y responsabilidad regulatoria.
Ver también: ¿Qué tratamientos celulares pueden considerarse legales y regenerativos?
¿Qué hace que las células mesenquimales cultivadas sean un medicamento de terapia celular avanzada?
Las células mesenquimales cultivadas (CMC) adquieren la consideración de medicamento de terapia celular avanzada cuando, tras su obtención, son sometidas a una manipulación sustancial mediante expansión ex vivo en condiciones controladas. Este proceso permite aumentar selectivamente la población mesenquimal, definir una dosis celular precisa y estandarizar el producto bajo criterios farmacéuticos.
La fabricación en sala blanca conforme a normativa GMP, la caracterización fenotípica, los controles de calidad y la supervisión regulatoria transforman el material biológico inicial en un medicamento de terapia celular avanzada. No se trata únicamente de administrar células, sino de desarrollar un producto celular con identidad farmacológica, trazabilidad y marco legal específico.
Es esta combinación de manipulación sustancial, control industrial y regulación sanitaria la que distingue a las células mesenquimales cultivadas de otros procedimientos biológicos y fundamenta su clasificación como medicamento de terapia celular avanzada en el contexto europeo.
¿Qué son los concentrados celulares del mismo día?
Los concentrados celulares obtenidos y aplicados en la misma intervención quirúrgica se caracterizan porque:
- No pasan por expansión en cultivo
- No aumentan la población específica de células mesenquimales
- No constituyen un medicamento de terapia avanzada
- No requieren fabricación GMP
- No implican autorización individual de la AEMPS como medicamento
Desde el punto de vista regulatorio europeo (Directiva 2001/83/CE) y nacional, estos productos no se consideran medicamentos de terapia celular avanzada cuando no existe manipulación sustancial .
Su naturaleza es distinta tanto en definición legal como en caracterización biológica.
Comparativa: concentrado del mismo día vs. células mesenquimales cultivadas

La diferencia clave no es el origen celular, sino el proceso:
| Característica | Concentrado mismo día | Células mesenquimales cultivadas |
| Manipulación | No sustancial | Sustancial (cultivo) |
| Dosis celular | No definida | Definida (20–120 millones) |
| Caracterización | No estandarizada | Fenotipo validado |
| Fabricación GMP | No | Sí |
| Regulación | Procedimiento | Medicamento |
La expansión celular permite:
- Multiplicar la población mesenquimal
- Controlar la dosis
- Garantizar reproducibilidad
- Evaluar calidad y viabilidad
Sin expansión, no existe un medicamento celular definido.
Ver también: Avances clínicos en tendinopatía rotuliana, aplicación de terapia avanzada con Células Mesenquimales Cultivadas (CMC)
Diferencia regulatoria: procedimiento vs. medicamento
En España y en el marco de la Unión Europea, un producto celular expandido ex vivo bajo condiciones de correcta fabricación (GMP) entra en la categoría de medicamento de terapia celular avanzada. Esta clasificación no depende de la intención clínica, sino del grado de manipulación y del proceso industrial aplicado al material biológico.
Las células mesenquimales cultivadas (CMC), al ser sometidas a expansión celular y caracterización controlada, adquieren identidad farmacológica propia. Dejan de ser un simple tejido autólogo procesado para convertirse en un medicamento sujeto a la legislación farmacéutica europea.
1. Manipulación sustancial y estatus jurídico
El punto de inflexión regulatorio es la manipulación sustancial. La expansión celular durante varias semanas, bajo condiciones controladas de laboratorio, implica:
- Aumento cuantitativo de la población mesenquimal
- Selección y purificación celular
- Definición de una dosis terapéutica
- Control de esterilidad, viabilidad y estabilidad
Este proceso sitúa al producto dentro del régimen jurídico de los medicamentos biológicos avanzados. No se trata de una interpretación conceptual, sino de una consecuencia directa de la normativa europea aplicable.
2. Implicaciones regulatorias obligatorias
La clasificación como medicamento de terapia celular avanzada implica una serie de requisitos estructurales:
- Dossier farmacéutico o PEI (Investigational Medicinal Product Dossier)
- Ensayo clínico autorizado cuando corresponde
- Programa de farmacovigilancia
- Supervisión y control por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)
- Certificado de Producto Farmacéutico (CPP)
Estos elementos no son opcionales. Constituyen el marco que garantiza trazabilidad, reproducibilidad y responsabilidad sanitaria.
3. Autorización individual y responsabilidad sanitaria
Cuando la aplicación de células mesenquimales cultivadas no se realiza dentro de un ensayo clínico autorizado, su uso requiere autorización individual de la AEMPS, conforme al régimen de medicamentos de terapia avanzada.
En ITRT, cada indicación se evalúa bajo este marco regulatorio, asegurando que el medicamento de terapia celular avanzada se administre con respaldo jurídico y farmacéutico adecuado.
La diferencia regulatoria entre un procedimiento biológico y un medicamento celular es, por tanto, estructural. Define el nivel de control sanitario, el grado de evidencia exigible y la responsabilidad profesional asociada a su aplicación clínica.
Ver también: ITRT presenta evidencias de regeneración tendinosa sin precedentes en el Swiss Medical Network Regenerative Day
Diferencia clínica: evidencia estructural
La diferencia clínica entre un procedimiento biológico y un medicamento de terapia celular avanzada con células mesenquimales cultivadas (CMC) no se basa únicamente en la técnica de administración, sino en el modelo de desarrollo científico que lo sustenta.
En el caso de ITRT, el desarrollo de medicamentos basados en células mesenquimales cultivadas ha seguido un programa clínico estructurado, con metodología propia de investigación farmacológica.
1. Desarrollo bajo ensayo clínico autorizado
El uso de CMC en ITRT ha incluido:
- Ensayos clínicos fase I–II
- Protocolos aprobados por Comité Ético (CEIm)
- Autorización por la AEMPS
- Seguimiento clínico protocolizado
Este marco permite evaluar seguridad, factibilidad y resultados bajo criterios científicos definidos previamente, con recogida sistemática de datos y análisis estadístico.
2. Publicación y revisión científica
Los resultados obtenidos con células mesenquimales cultivadas han sido publicados en revistas científicas indexadas, lo que implica:
- Revisión por pares
- Transparencia metodológica
- Acceso público a los datos clínicos
La publicación científica forma parte del ciclo de desarrollo de un medicamento celular avanzado y constituye un elemento diferenciador frente a intervenciones sin programa estructurado de investigación.
3. Evaluación objetiva mediante imagen
En determinadas indicaciones, la evaluación clínica se ha complementado con estudios de resonancia magnética para documentar cambios estructurales. Esta aproximación permite analizar no solo la evolución sintomática, sino también modificaciones tisulares objetivables por imagen.
La documentación de regeneración estructural mediante resonancia forma parte del diseño metodológico de algunos ensayos desarrollados con CMC.
4. Ausencia de programa farmacológico en concentrados del mismo día
Por el contrario, los concentrados celulares aplicados en el mismo acto quirúrgico no han sido desarrollados como medicamentos con programa clínico farmacológico completo. No forman parte de un itinerario que incluya dossier farmacéutico, fases de ensayo clínico ni estrategia de farmacovigilancia propia de un medicamento biológico avanzado.
La diferencia no es de intención terapéutica, sino de marco científico y regulatorio. Es la existencia de un programa de desarrollo farmacológico lo que define el nivel de evidencia exigible y la solidez metodológica del medicamento de terapia celular avanzada.
Sobre el término “células madre”
En el lenguaje divulgativo se utiliza con frecuencia el término “células madre mesenquimales” para describir distintas intervenciones biológicas. Sin embargo, esta expresión no distingue entre un concepto biológico general y un producto desarrollado bajo normativa farmacéutica.
Cuando estas células son aisladas, expandidas y fabricadas en condiciones GMP, constituyen el principio activo de un medicamento de terapia celular avanzada. En ese contexto regulado, el término correcto es células mesenquimales cultivadas (CMC).
La precisión terminológica no es secundaria: define el estatus jurídico del producto, el marco regulatorio aplicable y el nivel de control sanitario exigido.
Más allá del tejido de origen: el verdadero factor diferenciador
No todas las intervenciones biológicas derivadas de médula ósea son equivalentes.
La diferencia entre un concentrado celular aplicado el mismo día y un medicamento de terapia celular avanzada con células mesenquimales cultivadas (CMC) reside en elementos estructurales:
- La manipulación sustancial
- La fabricación bajo normativa GMP
- La definición y estandarización de la dosis
- La regulación farmacéutica aplicable
- La existencia de evidencia clínica estructurada
Comprender esta distinción es esencial para interpretar con rigor el alcance científico, clínico y regulatorio de cada enfoque. No se trata de una variación técnica, sino de una diferencia que determina el nivel de control sanitario y el modelo de desarrollo biomédico implicado.
En ITRT, cada caso se evalúa dentro de un marco estrictamente médico y normativo. Si desea conocer si su situación clínica puede ser valorada conforme a estos criterios, puede solicitar una consulta médica para estudio individualizado.
No. Las células mesenquimales cultivadas son un medicamento fabricado bajo normativa GMP y autorizado por la AEMPS. Un concentrado del mismo día es un procedimiento sin expansión celular.
Preguntas frecuentes
No. Las células mesenquimales cultivadas son un medicamento fabricado bajo normativa GMP y autorizado por la AEMPS. Un concentrado del mismo día es un procedimiento sin expansión celular.
No, salvo que exista manipulación sustancial y fabricación bajo normativa farmacéutica.
Cuando constituyen un medicamento de terapia celular avanzada, su uso se realiza bajo ensayo clínico autorizado o autorización individual regulatoria.
Aviso legal obligatorio
Medicamento de terapia celular avanzada (CMC), sujeto a prescripción médica y autorización individual por la AEMPS. Contenido divulgativo, no sustitutivo del consejo médico.